研究成果(共同)「藍藻間で硫酸化多糖の合成系を移植し 機能させることに成功」 | バイオサイエンス学科 渡辺 智 教授ら
2026年4月28日
教育・学術

藍藻間で硫酸化多糖の合成系を移植し 機能させることに成功
-光合成による有用多糖バイオものづくりに新展開-
【ポイント】
- ・研究グループが過去に同定した藍藻硫酸化多糖であるシネカンの合成と制御に関わる遺伝子群を、別の藍藻に導入して機能させることに成功
- ・その結果、硫酸化多糖を産生しない藍藻種に、硫酸化多糖の産生能を付与
- ・光合成を利用したバイオものづくりの将来に向けて、藍藻により有用多糖類を生産する戦略の可能性を示した
【概要】
東京科学大学(Science Tokyo) 総合研究院 化学生命科学研究所の前田海成助教と東京農業大学 生命科学部 バイオサイエンス学科の渡辺智教授らの研究チームは、光合成微生物である藍藻(シアノバクテリア、用語1)において、硫酸化多糖(用語2)を産生しない種に、別の種が持つ多糖の合成・制御を行う複雑な仕組みを導入し、実際に硫酸化多糖を産生させることに成功しました。今回導入したのは、研究グループが解明してきた、藍藻の硫酸化多糖であるシネカン(用語3)の合成と制御に関わる遺伝子群です。
コンドロイチン硫酸などに代表される硫酸化多糖は、医薬品や化粧品の原料など、さまざまな用途で活用されている有用な多糖類であり、その多くは動物由来です。一方で藍藻は、バクテリアの中では珍しく多くの種で多様な硫酸化多糖を作ることが知られており、硫酸化多糖の生産ホストや硫酸化多糖の合成に関わる遺伝子群の情報源となることが期待されています。
本研究は、藍藻に異種由来の硫酸化多糖の合成関連遺伝子群を導入することで硫酸化多糖を産生させた初めての研究です。本成果は、藍藻の光合成により有用な硫酸化多糖を生産する「持続可能なバイオものづくり研究」や、未知の硫酸化多糖および関連遺伝子の機能を「人工的に作って解明する合成生物学的研究」に向けた第一歩となるものです。
本成果は、4月28日付(現地時間)の「Scientific Reports」誌に掲載されました。
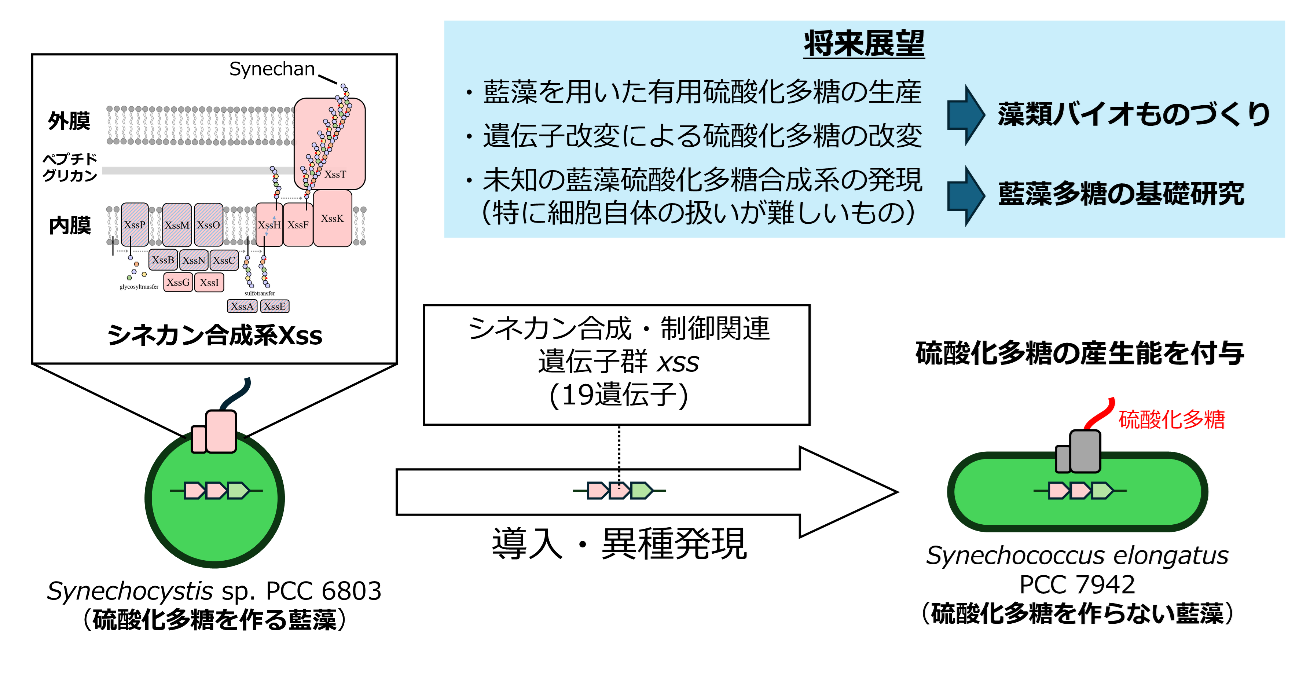
図1 本研究の概要図
●背景
硫酸基で修飾された多糖である硫酸化多糖は、コンドロイチン硫酸やヘパリンなどに代表されるように、医薬品や化粧品の原料など幅広い用途で活用されている有用物質です。現在利用されている硫酸化多糖の多くは動物由来であるため、安定供給や持続可能性、新規分子の開拓や組成・機能の改変の観点から、近年は微生物を利用した生産技術の開発が求められています。
藍藻(シアノバクテリア)は植物と同様に酸素発生型の光合成を行い、二酸化炭素を固定して増殖するバクテリアの一群です。地球環境を支える重要な生物群であるだけでなく、持続可能なバイオものづくりの生産を担うホスト(宿主)としても注目されています。さらに、硫酸化多糖を作る既知のバクテリアが限られている中で、藍藻の多くは多様な硫酸化多糖を生産することが知られています。そのため藍藻は、天然の硫酸化多糖の資源であるというだけでなく、異種由来の硫酸化多糖の生産ホストや、硫酸化多糖の合成や制御に関わる遺伝子群の情報源としても期待されています。
これまでに研究チームは藍藻の1種が作る硫酸化多糖であるシネカンを発見し、その研究により藍藻硫酸化多糖の合成と制御に関わる遺伝子群を世界で初めて同定しました[参考文献1]。一方で、ある藍藻種が持つ硫酸化多糖の複雑な生産系を別の藍藻種へ移して機能させられるかどうか、つまり機能的な異種発現が可能なのかは不明でした。
●研究成果
本研究では、シネカンの合成と制御に関わるxss遺伝子群を、研究チームが開発した高発現シャトルベクター(用語4)[参考文献2]のpYSを用いて硫酸化多糖を産生しない藍藻種であるSynechococcus elongatus PCC 7942 に導入しました(図1)。
xss遺伝子群はシネカンの合成・制御に関わるさまざまな機能を持つ遺伝子が集合した巨大な遺伝子クラスターです。この遺伝子クラスターを協調的に動かすために、xss遺伝子群の転写を制御するXssRとXssQというタンパク質をコードする遺伝子も同時に導入してクラスター全体の発現を試みました。RNA-seq解析(用語5)により、xss遺伝子群を導入した株では発現誘導条件において目的遺伝子群の発現が確認されました。また、細胞外に多糖の蓄積がみられ(図2下)、その組成分析により硫酸化多糖の存在が確認されました。つまり、藍藻硫酸化多糖の機能的な異種発現に成功しました。しかし、得られた硫酸化多糖は、元の藍藻が作るシネカンと完全には同一でなく単糖組成に違いが見られました。この結果は、完全に再構成するには遺伝子発現の最適化を含めた今後の研究が必要であることを示しています。一方で、藍藻硫酸化多糖の合成系を改変すれば、作られる多糖の組成を変えられる可能性を示しています。

図2 作製した株の走査型電子顕微鏡像
●社会的インパクト
本成果は、藍藻由来の硫酸化多糖の複雑な生産系を、別の藍藻種に移して機能させられる可能性を初めて実証したものです。これは、藍藻を用いた有用多糖のバイオものづくりへの重要な一歩といえます。硫酸化多糖には付加価値の高いものが多く知られているため、社会実装に適した物質生産技術の開発ターゲットの1つです。本研究はまだ始まったばかりですが、将来的には、医薬品の原料になるような高付加価値の硫酸化多糖を、藍藻を用いた光合成により二酸化炭素を原料として生産することで、動物資源への依存を低減しつつ有用多糖類の持続可能な生産を達成できる可能性があります。
●今後の展開
今後は、作製した株や遺伝子発現系の改良と、シネカンや合成された硫酸多糖の解析を進めることで、異種に導入した硫酸化多糖合成系が正常に機能するのに必要な条件の詳細な解明を目指します。また本研究は、藍藻を用いた有用多糖生産の基盤技術としてだけでなく、未知の多様な藍藻硫酸化多糖の合成遺伝子群や機能を異種の藍藻で発現させ再構成し解析することで「人工的に作って解明する合成生物学的研究」の足がかりにもなります。藍藻の硫酸化多糖合成系を深く理解することは、藍藻がいつ、どのように、何のために硫酸化多糖を生産しているのかを明らかにする基礎研究において非常に重要です。さらに、得られる知見を基に、多様な硫酸化多糖の合成遺伝子群を組み合わせることで、天然には存在しない新たな構造や性質を持つ多糖を設計・生産する応用研究にもつながると期待されます。
●付記
本研究は、日本学術振興会 特別研究員奨励費JP19J01251、JST ACT-X 「環境とバイオテクノロジー」領域JPMJAX20BG、および東京農業大学生物資源ゲノム解析センターの共同研究助成の支援を受けて実施されました。
【参考文献】
[1] Maeda, K., Okuda, Y., Enomoto, G., Watanabe, S. & Ikeuchi, M. Biosynthesis of a sulfated exopolysaccharide, synechan, and bloom formation in the model cyanobacterium Synechocystis sp. strain PCC 6803. Elife. 10, e66538 (2021).
[2] Sakamaki, Y., Maeda, K., Nimura-Matsune, K., Chibazakura, T. & Watanabe, S. Characterization of a cyanobacterial rep protein with broad-host range and its utilization for expression vectors. Front. Microbiol. 14, 1111979 (2023).
【用語説明】
(1) 藍藻(シアノバクテリア):酸素発生型の光合成により二酸化炭素を固定して増殖するバクテリアの一群。有機物や酸素の供給者として地球環境にとって重要な生物であるだけでなく、光合成による持続可能なバイオものづくりのホスト生物としても注目されている。
(2) 硫酸化多糖(硫酸多糖):硫酸基で修飾された多糖類で酸性多糖の仲間。硫酸基由来の負電荷を持ち、保水性や粘性、生理活性を示すものが多く知られている。自然界における代表的な生産者は動物、真核藻類、藍藻である。
(3) シネカン:淡水性モデル藍藻Synechocystis sp. PCC 6803が生産する硫酸化多糖。当研究グループが2021年に報告した。現時点で合成・制御遺伝子群が同定されている唯一の藍藻硫酸化多糖である。b(4) シャトルベクター:複数の種の中で複製が可能なベクター。本研究で使用したpYSベクターはシアノバクテリアの細胞内にたくさん存在している高コピープラスミド由来の複製機構を持っており、導入した遺伝子を高いレベルで発現させることができる。
(5) RNA-seq解析:細胞内のmRNA量を網羅的に測定し、遺伝子発現の変化を解析する手法。
【論文情報】
掲載誌:Scientific Reports
論文タイトル:Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942.
著者:Kaisei Maeda*, Kazuma Ohdate, Yutaka Sakamaki, Kaori Nimura-Matsune, and Satoru Watanabe*
DOI:10.1038/s41598-026-46439-4
